まいらいふのページ

2009年 「まいらいふ」8月号
| 骨髄異形成症候群 |
| 「骨髄異形成症候群」は聞き慣れない病名だと思います。「骨髄」は骨の内部にあり血液の細胞を造る造血組織、「異形成」は造血に異常があることを意味し、単一の病気ではないと考えられているため「症候群」と付いています。実は比較的頻度が高く、10万人あたりの年間発症率は2?3人以上。熊本県では毎年50人前後の方が発症する計算になります。高齢者に多いため年々増加しています。今回は、良い治療法がなく難病とされてきた骨髄異形成症候群とその新しい治療法を紹介します。 |
| 造血の仕組み |
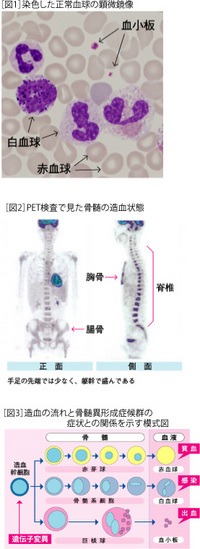
血液中には赤血球、白血球、血小板の三種類の細胞が流れています(図1)。これらの細胞はみな骨髄で造られます(図2)。再生医療で幹細胞という名前を聞いたことがあるかと思いますが、骨髄には「造血幹細胞」があり、これら三種類の血球を造ります。骨髄の中で造血幹細胞から生まれた未熟細胞が成熟細胞へと姿を変え、血液へ出てきます(図3)。造る血球の数は造血因子によって精妙に調節されています。 |
| どんな病気? |
|
英語ではMDSと略される骨髄異形成症候群は、骨髄での造血がおかしくなる病気です。骨髄では血球を作ろうとするのに正常に作れなくて血液中の血球が減少します。「無効造血」と表現されますが、異常な形の細胞がみられ、「異形成」と呼ばれるゆえんです。一血球とは限らず、三血球とも減少したりしますので、造血幹細胞の異常です。原因はまだよく分かっていません。被爆者や、がんで抗癌剤や放射線治療を受けた方に多く発症しますので、造血幹細胞の遺伝子に異常が生じて発症すると考えられています(図3)。その証拠に、この病気の骨髄細胞では遺伝子の集まりである染色体の異常が少なからず見つかります。遺伝子の異常は、健常者の正常細胞でも複製の際にある頻度で生じますが、修復されたり、排除されたりして正常に保たれています。加齢でその修復機能が衰え、他方で遺伝子異常が起きる頻度が増加した場合に、その異常が集積されて発症すると考えられます。 |
| これまでの治療 |
|
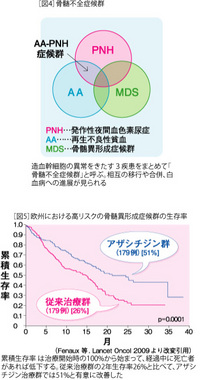
芽球と言われる未熟細胞が多いほど白血病へ移行するリスクが高くなります。芽球が少ない低リスクの患者さんでは進行も緩やかで、輸血などの補助療法が主に行われます。高リスクの患者さんでは白血病に準じた抗癌剤治療が行われます。しかし、その効果は乏しく生命予後は不良です。唯一、造血幹細胞移植が根治的な治療法です。移植は一般的には55歳以下で可能な治療ですので、残念ながら、年齢的に多くの方で実施ができません。 |
| 新しい治療法 |
長年にわたる輸血は、赤血球に含まれる鉄分が体内で過剰となって各臓器に沈着し、心不全や肝障害などを起こします。昨年、日本でも経口の除鉄剤が認可され、長期間安全に輸血を行えるようになったことは朗報です。 |

熊本大学大学院
医学薬学研究部 血液内科学分野 准教授 麻生範雄 |